Op 17 November publiceerde De Limburger een artikel over de Finse Hanna, die nu in Vlaanderen woont, en positief resultaat ondervond van de stamcelbehandeling in het Maastricht UMC+.
Lees het hele artikel hieronder:
Op 17 November publiceerde De Limburger een artikel over de Finse Hanna, die nu in Vlaanderen woont, en positief resultaat ondervond van de stamcelbehandeling in het Maastricht UMC+.
Lees het hele artikel hieronder:
De aanwijzing van deze expertisecentra moet zorgvuldig plaatsvinden. De afgelopen jaren heeft een grote groep patiëntenorganisaties veel kritiek geleverd op de inrichting en uitvoering van de procedure. De beleidsvisie 2025 biedt helaas geen oplossing voor de ervaren problemen en zet de patiënt met een zeldzame aandoening nog verder op achterstand.
Benieuwd naar de reflectie? zie bijgevoegd document.
Deze reflectie wordt ondersteund door:
Stichting 1 op 5
Stichting Huidlymfoom
Patiëntenvereniging Ziekte van Hirschsprung
NFVN
ITP Patiëntenvereniging Nederland
CMTC-OVM
Stichting Orthostatische Tremor
PlatformCHD
VOKS
Nevus Netwerk Nederland
Nederlandse Hypofyse Stichting
EDS-FONDS
Vereniging van Huntington
Nederlandse Klinefelter Vereniging
Patiëntenvereniging Fibreuze Dysplasie
Vereniging voor Angio-oedeem
Patiëntenplatform Sarcomen
Patiëntenvereniging HEVAS
Belangenvereniging LOA/LHON
Power of Reflection
Stichting NeMo
Meer dan de helft van de patiënten met een m.3243A>G mutatie, onder wie dragers van MELAS en MIDD, is snel vermoeid en heeft spierzwakte. Hiervoor is op dit moment geen therapie beschikbaar. In het Maastricht UMC+ wordt onderzocht of toediening van spierstamcellen kan leiden tot verbetering van de spierfunctie. Om afstotingsreacties te voorkomen gebruiken de onderzoekers hiervoor patiënt-eigen spierstamcellen. In het laboratorium hebben zij aan de hand van spierbiopten aangetoond dat ongeveer de helft van de m.3243A>G mutatiedragers mutatievrije stamcellen heeft. In de fase I veiligheidsstudie zijn in het MUMC patiënt-eigen spierstamcellen opgekweekt en 1 maal door toediening via een arterie van het onderbeen aan de patiënt teruggegeven. Een dergelijke studie is noodzakelijk om te kunnen aantonen dat de toediening veilig is en leidt tot vorming van nieuwe spiervezels. Deze eerste fase is succesvol afgerond.
In de volgende fase van de klinische studie, fase IIa, wordt nu onderzocht of 3 maal toediening van patiënt-eigen spierstamcellen in de bovenarm een effectieve dosis is en inderdaad leidt tot verbetering van de spierkracht en vermindering van de vermoeidheid. Deze therapeutische toediening vindt momenteel alleen plaats in studieverband. Als u graag meer informatie over dit onderzoek wilt ontvangen, maak dit dan kenbaar via het contactformulier.
Op 25 november 2023 publiceerde De Limburger een uitgebreid artikel over ‘Generate Your Muscle’ en het onderzoek naar de effectiviteit van stamcellen voor het herstel van beschadigde spieren.
Het volledige artikel is via deze link te lezen of door op onderstaande afbeelding te klikken.
De KSBS (Katholieke Stichting voor Blinden en Slechtzienden) interviewde dr. de Coo over autosomale dominante opticusatrofie (ADOA). “Of je nu een patiënt bent, een medische professional of gewoon nieuwsgierig bent naar medische vooruitgang, dit interview biedt waardevolle informatie over ADOA.” Aldus Cure ADOA foundation.
Je leest het gehele interview hier.

Het jaarraport van Stichting NeMO (Stichting voor Neuromusculair en Mitochondrieel Onderzoek) voor het boekjaar 2021 is gepubliceerd. Stichting NeMO is opgericht met als doel onderzoek te doen naar, en therapieën en behandelingen te ontwikkelen voor, zeldzame ziektebeelden.
In het jaarraport worden de projecten en initiatieven van het afgelopen jaar toegelicht, vindt u onze plannen voor de toekomst en maken we ook de jaarrekening inzichtelijk.
Op zaterdag 27 augustus organiseerde de familie Heijster een Fancy Fair bij de Voornse Hoeve in Oostvoorne. Deze dag konden bezoekers onder andere terecht voor eigen gemaakt gebak, bloemen, frietjes, een loterij, rommelmarkt en oud-Hollandse spellen. De opbrengst van deze dag werd geschonken aan Stichting NeMO.
Maarliefst €2287,- werd op deze dag opgehaald en zal worden gericht op het onderzoek aangaande de ziekte mutatie POLG1.
Deze foto’s geven een impressie van de dag:
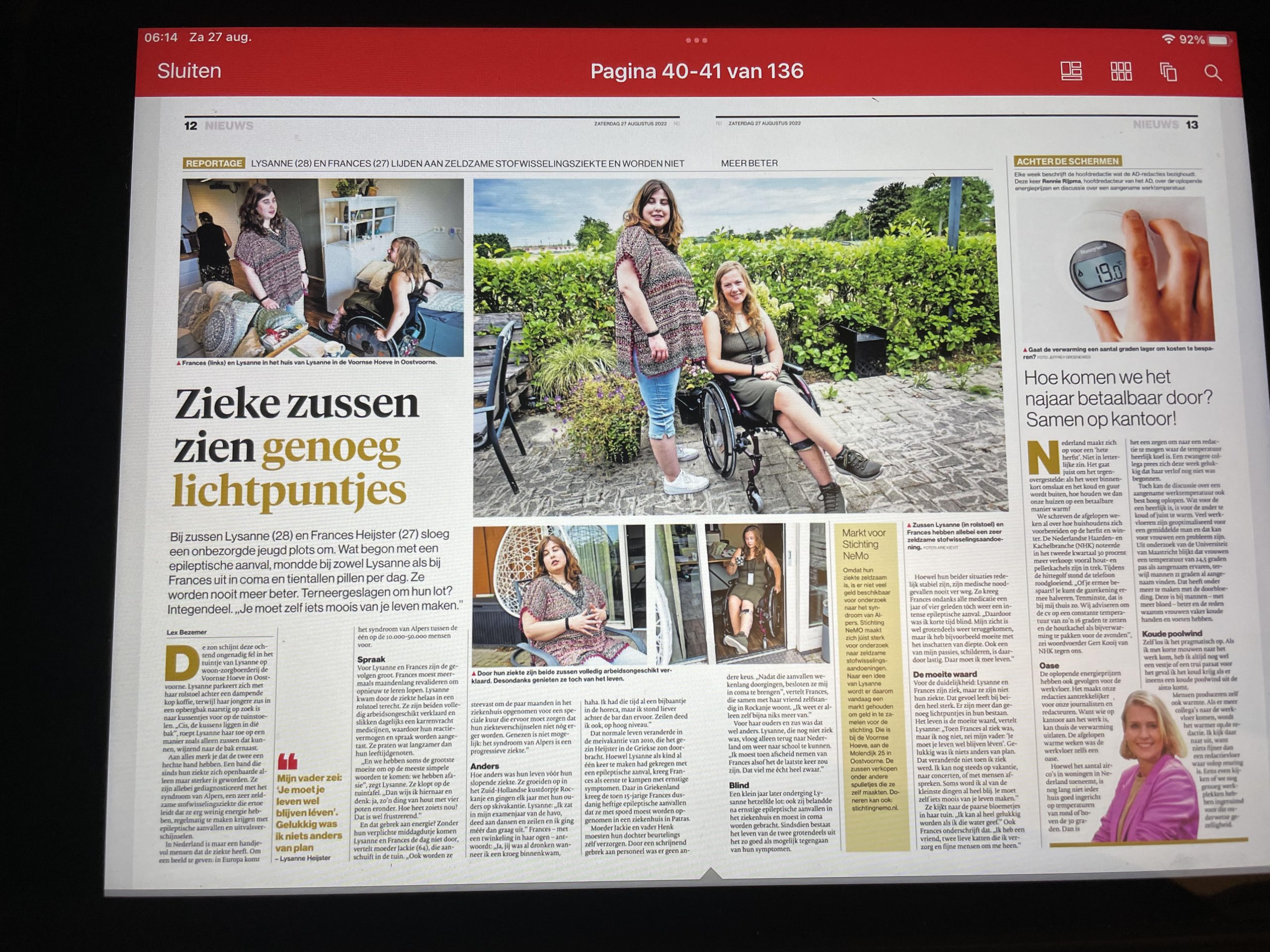
Eerder schonk het AD al aandacht aan de zussen Lysanne en Frances, het artikel kun je hieronder lezen.
Voor het eerst krijgen patiënten met een erfelijke spieraandoening gezonde lichaamseigen spierstamcellen toegediend. Dit biedt hoop voor patiënten met een erfelijke spierziekte. Het is een uniek onderzoek uitgevoerd door specialisten van een consortium onder leiding van Maastricht University. Stichting NeMO steunt het onderzoek.
De Nederlandse pers heeft er op verschillende manieren aandacht aan gegeven. Meer informatie over de trial is te vinden in het dit eerder gepubliceerde artikel.

Het jaarraport van Stichting NeMO (Stichting voor Neuromusculair en Mitochondrieel Onderzoek) voor het boekjaar 2021 is gepubliceerd. Stichting NeMO is opgericht met als doel onderzoek te doen naar, en therapieën en behandelingen te ontwikkelen voor, zeldzame ziektebeelden.
In het jaarraport worden de projecten en initiatieven van het afgelopen jaar toegelicht, vindt u onze plannen voor de toekomst en maken we ook de jaarrekening inzichtelijk.
Vandaag, 28 februari 2022, is het ‘Rare Disease Day’. De dag waarop we wereldwijd stilstaan bij zeldzame ziekten. Er zijn in totaal 300 miljoen mensen die te maken krijgen met een zeldzaam ziektebeeld, hier zijn er zo’n 7000 verschillende van. Stichting NeMO zet zich in voor deze kleine patiëntengroepen. Op de website lees je meer over welke initiatieven de stichting steunt en aan welke ziektebeelden deze gerelateerd zijn.
Eén van de onderzoeken die wordt gesteund vanuit Stichting NeMO is ‘Generate your Muscle’, hierover vind je meer via: www.generateyourmuscle.com.
Lees deze pagina als je meer over de stichting te weten wilt komen.